根据《化妆品卫生监督管理条例》,使用化妆品新原料生产化妆品,必须经国务院卫生行政部门批准。化妆品新原料是指在国内首次使用于化妆品生产的天然或人工原料。从2004年至今,一共批准了10个新原料(详见表1)。
表1 2004-2016年批准化妆品原料
| 原料名称 | 批准时间 |
| 十六烷基三甲基氯化氨 ALKYL(C12-22)TRIMONIUM CHLORIDE(BROMIDE) |
2004年6月14日 |
| 甲氧基水杨酸钾 Potassium Methoxysalicylate |
2007年4月26日 |
| 9.69%甲基异噻唑啉酮 9.69% Methylisothiazolinone |
2007年5月28日 |
| 左旋肉碱酒石酸盐 Carnitine(and)Tartaric Acid |
2008年6月3日 |
| 香甜豌豆花提取物 LATHYRUS ODORATUS FLOWER EXTRACT |
2008年8月6日 |
| 低聚果糖 FRUCTOOLIGOSACCHARIDES |
2008年8月6日 |
| 聚甲基丙烯酰基赖氨酸 POLYMETHACRYLOYL LYSINE |
2012年3月19日 |
| 二甲氧基甲苯基-4-丙基间苯二酚 Dimethoxytolyl Propylresorcinol |
2012年3月19日 |
| 苯乙基间苯二酚 Phenylethyl Resorcinol |
2012年12月5日 |
| 翅果(Elaeagnus mollis diel)油 Elaeagnus mollis diel Oil |
2014年10月30日 |
由国家食品药品监督管理总局保健食品审评中心网站数据汇总显示,自2010年至2016年间,申请注册的化妆品新原料约181个(汇总数据见表2,3)。而这期间批准使用的化妆品新成分只有4个。
表2 2010-2016年 进口化妆品新原料注册数据汇总
| 年份 | 首次申请 | 补延 | 复核 | 总计 |
| 2010(6-12月) | 20 | 3 | 0 | 23 |
| 2011 | 48 | 36 | 3 | 87 |
| 2012 | 40 | 22 | 3 | 65 |
| 2013 | 13 | 36 | 5 | 54 |
| 2014 | 11 | 44 | 1 | 56 |
| 2015 | 7 | 31 | 2 | 40 |
| 2016 | 13 | 31 | 0 | 44 |
| 总计 | 152 | 203 | 14 | 369 |
由表2看出,2010-2012年进口化妆品新原料申报量平均每年约40个,但2013-2016年间首次申请量平均每年约10个。2011年7月1日,《化妆品新原料申报与审评指南》正式实施,这推动了企业在这期间开展申报工作。但结果显示该指南文件并没有提高新原料审批的批准率。
表3 2010-2016年 国产化妆品新原料注册数据汇总
| 年份 | 首次申请 | 补延 | 复核 | 总计 |
| 2010(6-12月) | 1 | 0 | 0 | 1 |
| 2011 | 5 | 4 | 0 | 9 |
| 2012 | 6 | 1 | 0 | 7 |
| 2013 | 5 | 3 | 0 | 8 |
| 2014 | 4 | 3 | 1 | 8 |
| 2015 | 5 | 3 | 1 | 9 |
| 2016 | 3 | 4 | 1 | 8 |
| 总计 | 29 | 18 | 3 | 50 |
相比进口化妆品新原料申报量,国产化妆品新原料申报量少了很多。平均每年约5个。翅果油为最近被批准的一个国产化妆品新原料。
虽然化妆品新原料注册的技术要求不及药品注册,但时间成本已经相差无几。低批准率原因主要表现在以下几个方面:1)前期无统一的参考目录判定是否属于新原料;2)化妆品原料管理体系不完善,比如批准后的原料如何管理;3)动物实验数据要求与2013年欧盟全面禁止动物实验的化妆品法规相违背;4)实际审评要求远多于《化妆品新原料申报与审评指南》内容;5)无对外交流窗口可以直接与审评专家沟通讨论;6)美容产业技术创新的必要性不及药品和食品产业。国家食品药品监督管理总局自从卫生部接手化妆品卫生行政许可工作以来,虽然批准的新原料屈指可数,但可以看到政府为了更好更科学地管理化妆品原料市场,近年来已经逐步发布一些法规文件对外公开征求意见。以下汇总了历年化妆品原料管理的进展情况。
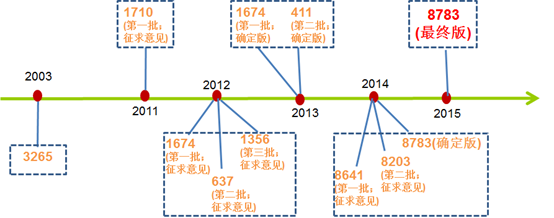
1)2011-2015.12.23: 完善化妆品原料目录正面清单(已使用化妆品原料目录IECIC)
2)2011.07.01:《化妆品新原料申报与审评指南》实施
3)2011.11.02:《关于进一步规范化妆品新原料行政许可有关事项的通知》(征求意见稿)
- 开展毒理学之前,实验室对原料定性、定量检验方法进行三批次样品的复核检验;
- 提交原料定性和定量检验方法、杂质的检验方法,不属于《化妆品卫生规范》、国家标准、行业标准和国家食品药品监督管理局印发的规范性文件中已有检验方法的,应提供完整的检验方法并同时提交不少于3家化妆品行政许可检验机构出具的相应检验方法的验证报告。
4)2014.01.23: 《关于调整化妆品新原料注册管理有关事宜的通告》(征求意见稿)
- 自2014年4月1日起,食品药品监管总局不再发布化妆品新原料审批公告。以《化妆品新原料试用批件》替代,批件有效期四年,有效期届满批件自行废止 。(审批公告制改为批件制)
- 获得批准的新原料可在批件核准的范围内生产、销售、使用。核准范围以外其它企业需使用该原料的,应当另行向食品药品监管总局申报 。(审批公告制导致批准的原料一旦公布,所有企业都可以进行生产,销售和使用。批件制可有效保护申请人的权益4年)
- 获得批准的申请人应当建立完整的化妆品新原料追溯制度及安全风险信息收集制度,通过食品药品监管总局建立的网络平台定期向食品药品监管部门报告新原料生产、流通、使用情况及安全相关信息 。(采取对申请人市场活动的市后监管)
- 批件有效期届满,结合使用情况进行评估符合要求的,食品药品监管总局将该新原料纳入已使用化妆品原料管理 。(4年有效期满后无安全问题的原料可纳入已使用化妆品原料目录)
5)2014.11.08: 《化妆品监督管理条例(征求意见稿)》
2015.07.20:《化妆品监督管理条例(修订草案送审稿)》
- 每年年底前重新发布更新后的目录;
- 高风险的新成分如防腐剂、染发剂、防晒剂、着色剂、美白剂等进行批准申请,其他成分在使用前30个工作日内提交备案;
- 经批准或备案的新原料,申请人或境内代理人应在3年内每半年提交新原料的使用及安全情况报告。
6)2015.11.10:调整植物类化妆品新原料行政许可申报资料要求公开征求意见
- 重新定义植物类化妆品新原料:指在我国境内首次使用于化妆品生产的植物(包括藻类)来源的天然原料。从植物中提取的单一成分或高度纯化的成分,不属于此定义范畴。
- 增加了毒理数据豁免条件。主要根据原料是否在国内外首次使用及提供五年以上安全使用或食用历史证明材料进行毒理数据豁免。
7)2015.11.10:《化妆品安全风险评估指南》(征求意见稿)
由2011-2015年间政府出台的一系列针对化妆品原料管理的文件推测,未来将基于保护申请人的权益根据原料风险程度进行分类管理。希望政府能够尽快实施之前颁布的文件,在下一个五年有更多的新原料能够合法用于中国市场。加快提高中国化妆品产业技术力量。瑞旭技术将于2017年6月28-29日在上海举办 第三届亚太化妆品法规峰会 。峰会将邀请国家食品药品监督管理总局的领导与专家对中国化妆品原料管理政策与趋势发表演讲。
UC的服务:
