为加强对进口化妆品的监管,国家药监局将组织开展对进口化妆品生产企业现场检查工作。本着公平竞争、国内国外一致原则,参照药品医疗器械境外检查相关工作程序。2019年5月,国家药监局着手起草了《化妆品境外检查暂行管理规定(征求意见稿)》(简称《规定》)。现于2019年11月22日向社会公开征求意见。公开征求意见的时间是 2019年11月22日—12月22日 。有关单位和个人可将意见反馈至hzpjgc@nmpa.gov.cn,请在电子邮件主题注明“化妆品境外检查暂行管理规定”。
《规定》正文共5章,36条,并附6个辅助性文件。
|
第一章 总则 (第一至第八条) |
|
第二章 检查计划和准备 (第九至第十五条) |
|
第三章 检查实施 (第十六至二十四条) |
|
第四章 审核及处理 (第二十五至三十三条) |
|
第五章 附 则(第三十四至三十六条) |
总则主要内容
- 化妆品境外检查定义
指国家药品监督管理局(以下简称国家局)为确认化妆品境外研制、生产相关过程及申报资料的真实性、可靠性和合规性所实施的境外现场检查。
- 主管当局
国家局:负责化妆品境外检查管理工作
国家局食品药品审核查验中心(简称核查中心):负责化妆品境外检查的具体组织实施
- 检查要求、基本情况和处理结果对外公开
- 检查员保守国家秘密、工作秘密和被检查单位的秘密
检查计划和准备主要内容
- 强调了境外检查基于风险控制的原则,优先选择在产品注册备案、检验、不良反应监测、投诉举报等环节发现有关问题,以及产品进口量大、在国内市场有较多消费者和较高影响度的企业进行检查。安全风险因素包括:
(一)审评审批过程发现潜在风险的;
(二)检验结果不符合规定,提示质量体系存在安全风险的;
(三)不良反应监测提示可能存在产品安全风险的;
(四)投诉举报或其他线索提示存在违法违规行为的;
(五)注册人或者备案人存在不良记录或失信行为的;
(六)境外监管机构公开信息提示注册人或备案人质量管理体系或产品存在较大风险的;
(七)其他需要开展境外检查的。
- 境外检查计划流程
境外检查工作语言为中文,注册人或者备案人提交的申报资料、整改报告等材料应当为中文版本,检查期间应当配备可满足检查需要的翻译人员。
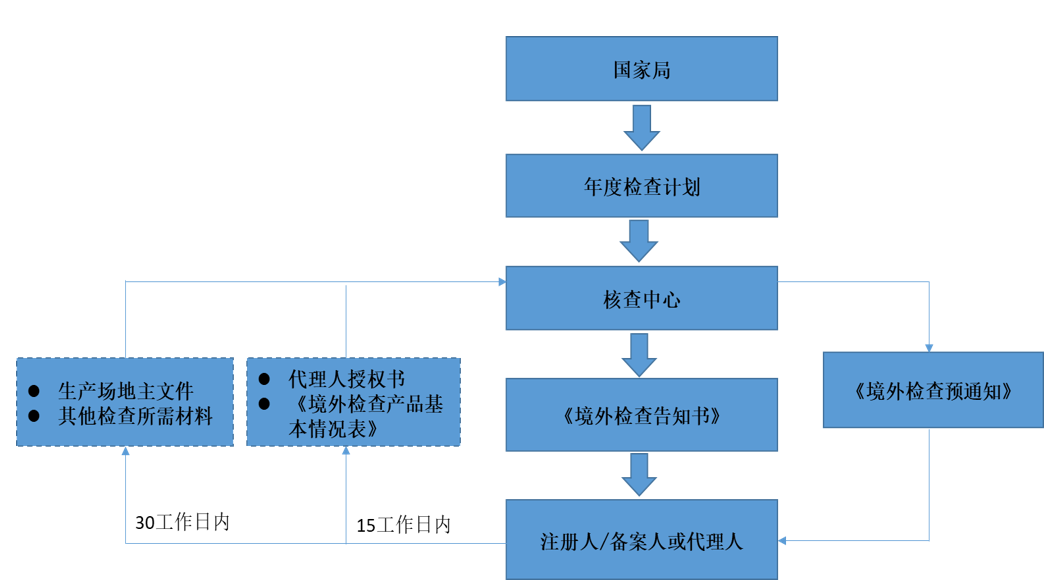
|
化妆品生产场地主文件:描述化妆品注册人或者备案人生产工厂或委托生产工厂质量管理体系的文件。 境外检查事务代理人:由注册人或者备案人指定1家中国境内机构(其在华分公司、办事处或代理商)。 代理人负责药品监管部门与注册人或者备案人之间的联络、承担化妆品不良反应监测、负责产品追溯召回等工作。代理人应当履行法律法规所规定的境内上市化妆品有关责任和义务,协助药品监管部门开展对产品境外研制、生产场地的检查和违法违规行为的查处。 |
检查实施主要内容
- 境外检查工作流程
检查组一般由3至5名检查员组成,检查组实行组长负责制。检查人员应当是依法取得国家级检查员资格的监管人员。检查人员应当签署无利益冲突声明、检查员承诺书和保密承诺书。
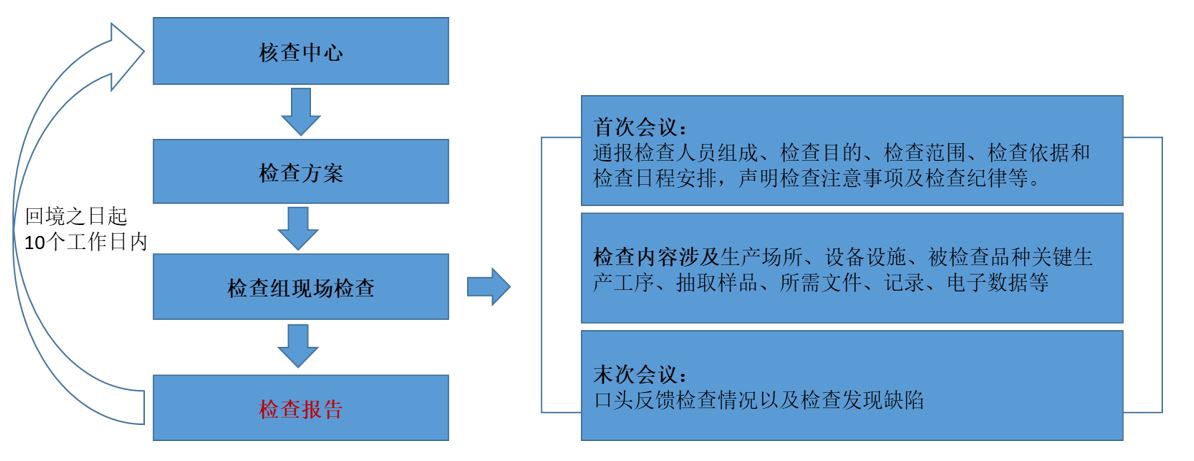
审核及处理主要内容
- 境外检查结果审核流程
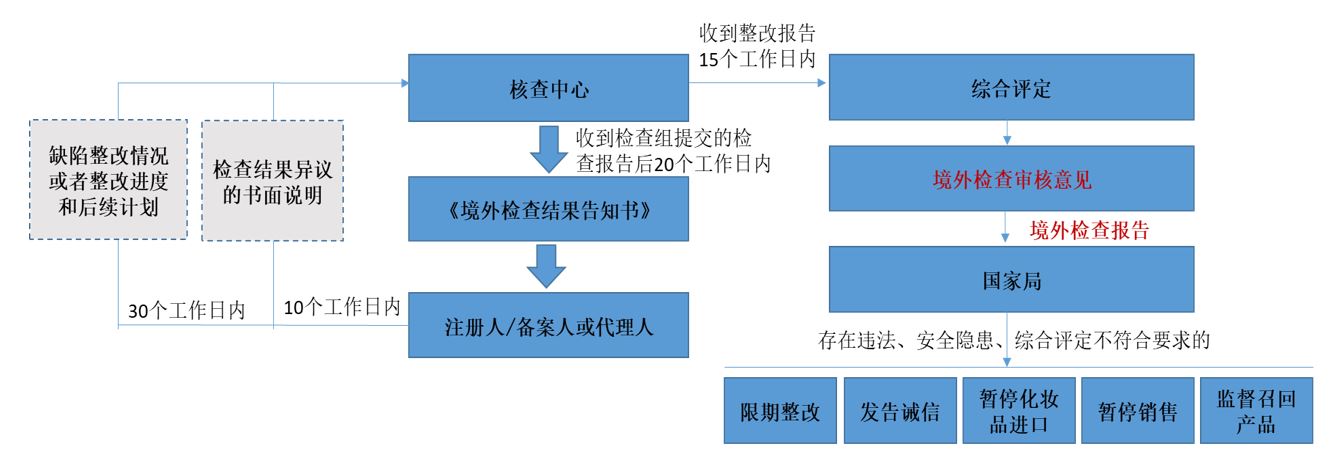
|
综合评定采用风险评估原则,综合考虑缺陷的性质、严重程度、频次以及产品的类别等。判定原则如下: (一)符合要求:现场检查未发现缺陷或仅发现轻微缺陷的。 (二)整改后符合要求:现场检查发现的所有严重缺陷和一般缺陷的整改措施,表明注册人或者备案人能够采取有效措施进行改正,能够按照法律法规及技术规范要求组织生产的。 (三)不符合要求:现场检查发现存在真实性问题、影响产品质量的关键要素与注册或备案资料不一致、生产质量体系存在《化妆品生产许可检查要点》5项以上(含5项)严重缺陷或者20项以上(含20项)一般缺陷、整改工作不到位等不符合法律法 规及技术规范要求的。 |
存在下列情形之一的,视为注册人或者备案人拖延、阻碍、限制或者拒绝检查,直接判定为“不符合要求”:
(一)《境外检查告知书》送达后,未在规定时限内提供符合要求代理人授权文件或其他要求的文件、资料的;
(二)注册人或者备案人拒绝或者两次推迟安排检查的;
(三)不配合办理境外检查手续的;
(四)拖延、阻碍、限制、拒绝检查人员进入被检查场所或者区域的,或者限制检查时间、设定不合理检查条件或者干扰检查的,或者不按照要求安排动态生产的;
(五)拖延、拒绝提供或者故意隐藏关键检查信息的;
(六)拒绝或者限制检查员收集证据相关资料的;
(七)其他不配合检查的情形。
附则主要内容
《规定》适用于香港特别行政区、澳门特别行政区和台湾地区注册人或者备案人的产品研制、生产相关过程的现场检查。
瑞旭评论
1) 根据《化妆品监督管理条例(征求意见稿)》第五十二条内容提到国务院药品监督管理部门可以对进口化妆品注册申报材料的真实性以及境外生产企业是否符合化妆品生产质量管理规范等要求,实施现场检查。该《规定》将作为即将出台的《化妆品监督管理条例》的配套法规文件。
2) 境外检查事务代理人的责任与进口非特备案境内责任人性质相同。但不同于进口特品的在华申报责任单位。
3) 国家局逐步统一国产与进口化妆品事后监管方式和要求。
4) 境外检查基于风险控制的原则,属于以下范围的产品或企业将作为政府优先选择的对象:a)产品注册备案资料存在真实性、可靠性和合规性风险的; b) 市场热度高的产品; c) 进口量大的产品;d) 安全风险较高的产品类型如婴幼儿、美白、防晒、染发等;e)信用不良企业;f) 知名品牌企业。
来源: 国家药监局综合司公开征求《化妆品境外检查暂行管理规定(征求意见稿)》意见
