为了进一步推进特殊医学用途配方食品注册工作,国家食品药品监督管理总局修订了《特殊医学用途配方食品稳定性研究要求(试行)(2017修订版)》,于2017年9月5日发布并实施。此类研究的目的是通过设计试验获得产品质量特性在各种环境因素影响下随时间变化的规律,并据此为产品配方设计、生产工艺、配制使用、包装规格和包装材料选择、产品贮存条件和保质期的确定等提供支持性信息。
为方便企业更直观的了解及应用《特殊医学用途配方食品稳定性研究要求(试行)(2017修订版)》,杭州瑞旭集团对其中的具体试验要求以及对提交材料的要求进行了归纳总结,具体内容如下所示:
1. 特医食品稳定性研究试验
稳定性研究应根据不同研究目的,结合食品本身的特性进行合理设置。其中,影响因素试验、加速试验和长期试验为必做试验;依据产品自身特点,可选择其他试验,例如开启后使用的稳定性试验等。
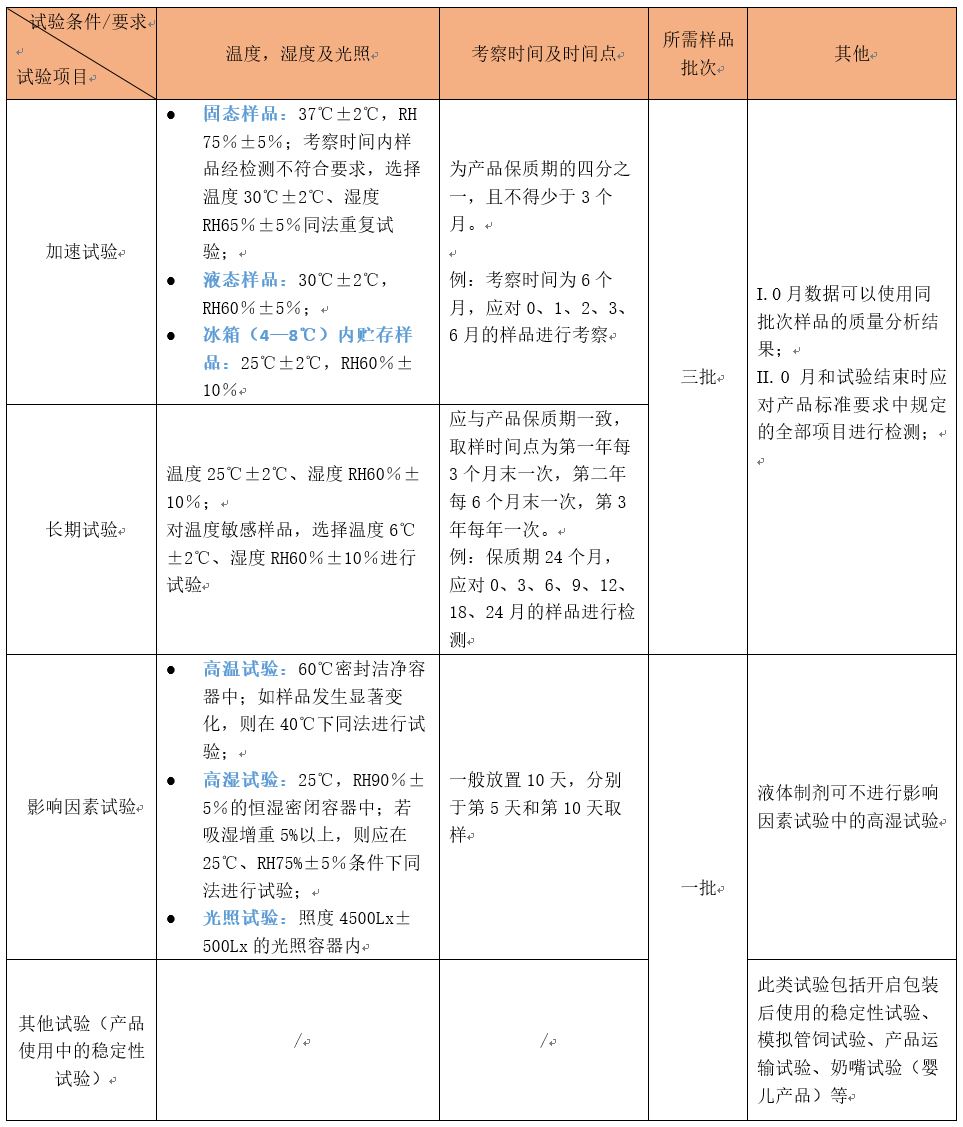
注:长期稳定性试验与加速试验应同时开始,申请人可在加速试验结束后提出注册申请,并承诺按规定继续完成长期稳定性试验。
2. 材料要求
产品注册申请时,申请人应当提交以下与稳定性研究有关的材料:
- 1) 试验样品的名称、规格、批次和批产量、生产日期和试验开始时间;
- 2) 不同种类稳定性试验条件,如温度、光照强度、相对湿度等;
- 3) 包装材料名称和质量要求;
- 4) 稳定性研究考察项目、分析方法和限度;
- 5) 以表格的形式提交研究获得的全部分析数据;
- 6) 各考察点检测结果,应以具体数值表示,其中营养成分检测结果应标示其与首次检测结果的百分比。计量单位符合我国法定计量单位的规定,不宜采用“符合要求”等表述。在某个考察点进行多次检测的,应提供所有的检测结果及其相对标准偏差(RSD);
- 7) 产品在贮存期内存在的主要风险、产生风险的主要原因和表现,产品稳定性试验种类选择依据,不同种类稳定性试验条件设置、考察项目和考察频率确定依据,稳定性考察结果与产品贮存条件、保质期、包装材料及产品食用方法确定之间的关系,对试验结果进行分析并得出试验结论。
注:稳定性试验报告与稳定性研究材料在产品注册申请时一并提交(对于特殊医学用途婴儿配方食品和全营养配方食品,申请人可保留记录备查,无需提交)。
更多关于特医食品注册的信息,请点击特殊医学用途配方食品注册
