由于疫情防控的需求,医用隔离鞋(套)也瞬间飙升为本季的明星产品,备受生产企业追捧。瑞旭集团医疗器械服务团队积极致力于协助企业完成应急刚需产品的备案,现将医用隔离鞋(套)产品的备案要求及流程分享如下:
1. 医用隔离鞋(套)产品概述
- 产品名称:医用隔离鞋、医用隔离鞋套
- 结构组成:采用适宜材料制成,有足够的强度和阻隔性能。非无菌提供。
- 工作原理:通过适宜材料,对接触到具有潜在感染性的患者血液、体液、分泌物等,起隔离、防护作用。
- 预期用途:医务人员在医疗机构中使用,防止接触到具有潜在感染性的患者血液、体液、分泌物等,起隔离、防护作用。
- 适用人群:适用于各种环境下需要进行防护的人群
- 预期使用环境:医疗机构、检验室
2. 医用隔离鞋(套)主要生产商

(来源:国家药品监督管理局-数据查询)
3.
医用隔离鞋(套)分类信息
|
子目录 |
一级 |
二级 |
产品描述 |
预期用途 |
品名举例 |
类别 |
|
14 注输、护理和防护器械 |
14 医护人员 |
05 足部 |
采用适宜材料制成,有足够的强度和阻隔性能。非无菌提供。 |
医务人员在医疗机构中使用,防止接触到具有潜在感染性的患者血液、体液、分泌物等,起隔离、防护作用。 |
医用隔离鞋、医用隔离鞋套 |
I |
医用隔离鞋(套)按照第一类医疗器械管理,需要根据要求完成医疗器械备案。
4.
医用隔离鞋(套)临床实验要求
医用隔离鞋(套)属于第一类医疗器械,免于进行临床试验,只需要提交临床评价资料。
5.
医用隔离鞋(套)技术要求
5.1 结构与规格
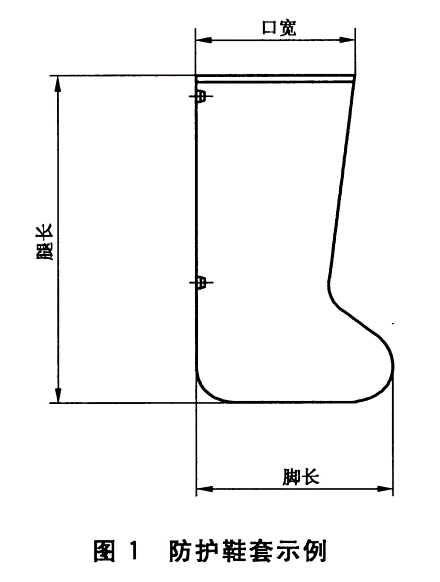
5.1.1防护鞋套的尺寸设计应能覆盖使用者的足部和腿部,起规格尺寸应符合标识的设计尺寸,允差±10%,防护鞋套的典型结构示例见图1。
5.1.2防护鞋套的结构应合理,穿脱方便。
5.1.3防护鞋套宜设计成带有收口的形式,可采用弹性收口、拉绳收口或绑带等收口方式
。
5.2 外观
5.2.1 防护鞋应无霉斑,表面不允许有杂质、黏连、裂缝、破损等缺陷。
5.2.2 鞋套的连接部位应平整、密合。
5.3 性能
5.3.1 抗渗水性
防护鞋套材料的静水压不应低于 1.67KPa ( 17cmH 2 O )。
5.3.2 抗合成血液穿透性
防护鞋套材料抗合成血液穿透性应不低于表 1 中 2 级的要求。
表 1 抗合成血液穿透性分级
|
级别 |
压强值 /Pa |
|
6 |
20 |
|
5 |
14 |
|
4 |
7 |
|
3 |
3.5 |
|
2 |
1.75 |
|
1 |
0* |
|
* 表示材料所受的压强仅为试验槽中的合成血液所产生的压强。 |
|
防护鞋套材料的外表面沾水等级应≥ 2 级。
5.3.4 断裂强力
防护鞋套材料的断裂强力应不小于 40N 。
5.3.5 断裂伸长率
防护鞋套材料的断裂伸长率应不小于 15% 。
5.3.6 过滤效率
防护鞋套材料及成品接缝处对非油性颗粒的过滤效率均应不小于 70% 。
5.4 微生物指标
5.4.1 非灭菌防护鞋套的微生物指标应符合表 2 的要求。
表2 防护鞋套微生物指标
|
细菌菌落总数 CFU/g |
大肠菌群 |
绿脓杆菌 |
金黄色 葡萄球菌 |
溶血性链球菌 |
真菌菌落总数 CFU/g |
|
≤ 200 |
不得检出 |
不得检出 |
不得检出 |
不得检出 |
≤ 100 |
5.4.2 包装上标志有“灭菌”或“无菌”字样或图示的防护鞋套应无菌。
5.5 环氧乙烷残留量
经环氧乙烷灭菌的防护鞋套,其环氧乙烷残留量应不超过10μg/g。
6、医用隔离鞋(套)适用的技术标准
|
GB/T 191-2008 |
包装储运图示标志 |
|
GB/T 15979-2007 |
一次性使用卫生用品卫生标准 |
|
YY/T 1633-2019 |
一次性使用医用防护鞋套 |
|
GB/T 4744 |
纺织品 防水性能的检测和评价 静水压法 |
|
GB/T 4745 |
纺织品 防水性能的检测和评价 沾水法 |
|
GB 19082-2009 |
医用一次性防护服技术要求 |
7、医用隔离鞋(套)备案时限
医用隔离鞋(套)作为第一类医疗器械,采用备案制,网上申请后现场提交备案资料,审核通过后,当场发放医用隔离鞋(套)备案凭证。
其中医用隔离鞋(套)备案凭证含两部分内容:第一类医疗器械备案凭证和第一类医疗器械备案信息表。
