UC 产品分类界定及注册策略
医疗器械分类管理
中国对医疗器械产品按照风险程度将其分为三类(即I类、II类和III类医疗器械),实行分类管理,不同类别的医疗器械产品,其注册、备案、许可程序及要求也不一样, 因此在医疗器械注册及相关许可申请之前确定产品分类是非常关键的。
-
I类医疗器械:风险程度低,实行常规管理可以保证其安全、有效的医疗器械。
-
II类医疗器械:具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械。
-
III类医疗器械:具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械。
医疗器械分类基于产品预期用途、作用机理、结构特征和使用途径,其类别确定主要根据医疗器械分类目录、分类规则来进行判定,对于涉及新技术、新结构、新材料等的医疗器械产品,必要时也可以进行分类界定申请,药品监督管理部门将组织专家对提交申请的产品进行分析评估并归类。
分类界定流程
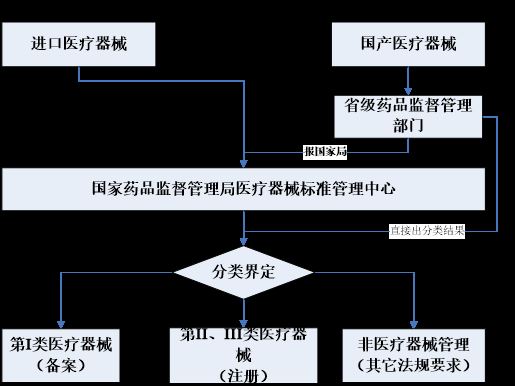
UC的服务
-
产品合规分析
-
法规调研报告
-
医疗器械分类界定申请
