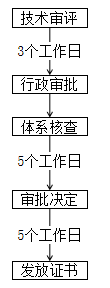
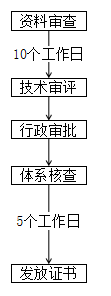
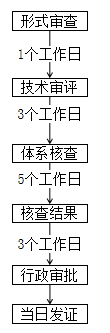
截止2022年9月,已有11个省份对医疗器械注册证转移政策发布了详细的法规政策及解读,本文汇总了各省医疗器械注册证迁入条件、简化流程及审批时限。
了解更多医疗器械注册快捷程序,请联系瑞旭集团医疗器械法规专家0571-87206527 或010-63984062。
|
省份 |
迁入条件 ( 政策链接后附 ) |
注册审批周期 |
|
天津 |
境内: ①外省市企业应在我市成立医疗器械生产企业(以下简称:入津企业),入津企业负责申报办理相关许可事项; ②外省市企业拟迁入我市产品为在外省市已获准注册的第二类医疗器械产品或已取得进口医疗器械注册证书的产品,同时符合我市医疗器械 “鼓励清单” 品种。 ③“鼓励清单”如下:
境外: ① 境外医疗器械产品(以下简称 “ 境外产品 ” )为国内按照第二类医疗器械管理的产品,同时符合我市医疗器械 “ 鼓励清单 ” 品种 ; ② 已取得国内进口医疗器械注册证书的产品;尚未取得国内进口医疗器械注册证书,但在境外已获准上市的产品; ③ 境外企业应指定我市企业法人作为其产品的注册申请人,负责申报办理产品入津注册事项。境内企业持有境外获准上市产品的适用本通知,应由境内企业自行申报产品注册。 |
境内:
境外:
|
|
河南 |
① 境内已注册第二类医疗器械品种因产业转移至我省,产品无实质改变、符合现行强制性标准,且注册检验合格的,申报注册时可采用原注册资料; ② 在我省具备生产条件且产品检验合格的,采信原审评审批意见, 合并审批生产许可和产品注册 。 |
- |
|
湖南 |
① 外省关联企业(与省内企业为同一法人、同一集团控股)在境内已注册的第二类医疗器械来湘申报注册的,产品无任何改变 , 管理体系符合要求,且产品检验合格的前提下 , 原则上认可原有的研究资料及注册信息。 ② 外省关联企业已完成研发尚未注册的第二类医疗器械来湘申报注册的 , 其研究过程及其结果符合注册要求,可提交已完成的研究资料 。 |
技术审评缩减至 5 个工作日 |
|
山东 |
同一集团 企业在境内 已注册第二类医疗器械 来鲁申报的,将原审评审批结论作为重要参考,加快核发医疗器械产品注册证和医疗器械生产许可证。 |
- |
|
广东 |
支持 已上市进口产品和省外产品 迁入我省注册。 境外 医疗器械注册人以 独资、合资或者合作方式 在我省设立的企业,以及 跨省兼并、重组或属同一集团 的 省内企业 (产品不发生实质性变化),进行第二类医疗器械注册申报时,可使用原产品注册时的有关申报材料。 |
原则上 技术 审评时限不超过 5 个 工作日 ; 质量管理体系核查时间另计 |
|
湖北 |
对 外省关联企业 在境内 已注册的第二类医疗器 械来鄂申报注册,产品无实质改变、符合现行法律法规及强制性标准,完成工艺验证且注册检验合格的,申报注册时可采用原注册资料,符合要求的,采信原审评审批意见,合并审批产品注册和生产许可。 |
原则上审评时限不超过 5 个 工作日,质量管理体系核查时间另计。 |
|
江苏 |
① 与已取得第二类医疗器械注册证的注册人隶属于同一集团。 ② 拟申报产品与同一集团已取得的注册证产品为同一品种器械,并在江苏境内生产。 ③ 根据现行的医疗器械分类目录、产品注册指导原则及有关分类界定文件,拟申报产品明确未第二类医疗器械。 ④ 注册申请人应为省内医疗器械生产企业。 ⑤ 拟申报产品为首次按照同一集团来苏注册程序进行申报的。如该产品存在因审批决定不予注册或注册申请人自行撤审的情形,该产品再次申报注册时按照常规程序开展审评审批。 |
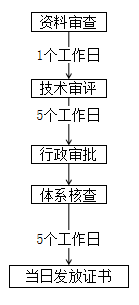
|
|
贵州 |
已在外省市取得产品注册证医疗器械生产企业,携已注册产品迁入本省生产的,在我省申请此类产品首次注册时, 除产品检验报告、生物相容性等研究性试验资料外 ,可使用原产品注册时的有关申报材料。 |
- |
|
辽宁 |
鼓励外省企业通过兼并、重组、资产注入、集团内转移、同一法人投资等方式,将已上市的第二类医疗器械转移至我省注册生产。符合上述情形的申请人,应当在申请注册时一并提交情况说明及证明材料,注册资料可使用原注册的相关内容。 |
按照辽宁省第二类医疗器械优先注册时限办理(原则上不超过 20个工作日) |
|
云南 |
加快集团内转移品种审评审批速度,对同一集团企业在境内已注册的第二类医疗器械来我省申请注册的,优化审评审批流程, 将原审评审批结论作为重要参考 ,提速医疗器械产品注册证和医疗器械生产许可证核发。 |
- |
|
江西 |
① 申请人与已取得第二类医疗器械注册证的注册人隶属于同一集团或同一法人。 ② 已取得的第二类医疗器械注册证必须符合现行法规规章要求。 ③ 拟申报产品与已取得的注册证产品为同一品种医疗器械,不发生实质变化,并在我省境内生产。 ④ 注册申请人应为省内医疗器械生产企业。 |
|
|
除本文所写受理条件以及资料准备,企业在进行注册证迁移时,最好向迁入省份进行电话沟通确认, 注册检测报告、产品技术要求 等较为重要文件是否允许资料互认。 |
||
各省医疗器械注册证迁入简化政策链接
|
省份名称 |
法规名称 |
发布日期 |
查询路径 |
|
天津 |
天津市药品监督管理局 关于印发天津市第二类医疗器械优先审批程序的通知 |
2019-11-10 |
天津市市场监督管理委员会 https://scjg.tj.gov.cn/tjsscjdglwyh_52651/zwgk/zfgznew/bdwwjnew/sjwwj_1/202012/t20201214_4995153.html |
|
天津市药品监督管理局关于简化外省市医疗器械企业产品迁入我市相关审批工作的通知 |
2020-01-31 |
天津市药品监督管理局 https://scjg.tj.gov.cn/tjsscjdglwyh_52651/tjyj/ZWGK149660/ZFGZ149668/gfxwjyjj/202012/t20201214_4995136.html |
|
|
天津市药品监督管理局关于优化境外医疗器械产品迁入我市有关审批事项的通知(试行) |
2022-06-29 |
天津市药品监督管理局 https://scjg.tj.gov.cn/tjsscjdglwyh_52651/tjyj/XWDT149660/GZTZ149685/202206/t20220630_5922294.html |
|
|
关于优化境外医疗器械产品迁入我市有关审批事项的通知》政策解读 |
2022-07-01 |
天津市药品监督管理局 https://scjg.tj.gov.cn/tjsscjdglwyh_52651/tjyj/ZWGK149660/ZFGZ149668/zcjdyjj/202207/t20220701_5923672.html |
|
|
河南 |
河南省药品监督管理局印发关于促进我省生物医药产业高质量发展的措施的通知
|
2021-03-21 |
河南省药品监督管理局 https://yjj.henan.gov.cn/2021/11-26/2355787.html |
|
湖南 |
湖南省药品监督管理局关于印发《医疗器械技术审评提质增效行动方案》的通知(湘药监发〔 2021〕30号) |
2021-09-02 |
湖南省药品监督管理局 http://mpa.hunan.gov.cn/mpa/xxgk/tzgg/wjtz/202109/t20210902_20456060.html |
|
湖南省药审中心为外省来湘企业提供精准技术咨询(一)、(二) |
2022-09-09 2022-09-12 |
(一) http://mpa.hunan.gov.cn/mpa/yszx/tpxw1/201909/t20190909_13968868.html (二) http://mpa.hunan.gov.cn/mpa/xxgk/gzdt/sjdt/201909/t20190912_5483261.html |
|
|
山东 |
《关于促进医疗器械产业高质量发展的十六条措施》 |
2022-05-13 |
山东省药品监督管理局 http://mpa.shandong.gov.cn/art/2022/5/13/art_101747_10324524.html |
|
政策解读:《关于促进医疗器械产业高质量发展的十六条措施》 |
2022-05-13 |
山东省药品监督管理局 http://mpa.shandong.gov.cn/art/2022/5/13/art_267473_10331163.html |
|
|
广东 |
广东省药品监督管理局办公室关于印发广东省药品监督管理局关于优化第二类医疗器械注册审评审批的若干措施的通知 |
2022-05-23 |
广东省药品监督管理局 -工作文件 http://mpa.gd.gov.cn/zwgk/gzwj/content/post_3935733.html |
|
关于已上市第二类医疗器械迁入我省注册申报指引(试行) |
2022-08-29 |
广东省药品监督管理局 -通知公告 http://mpa.gd.gov.cn/xwdt/tzgg/content/post_4002773.html |
|
|
湖北 |
深入开展 “下基层察民情解民忧暖民心”实践活动 进一步优化第二类医疗器械注册审评机制的若干措施 |
2022-05-27 |
湖北省药品监督管理局 http://mpa.hubei.gov.cn/zfxxgk/zc/qtzdgkwj/qtwj/202205/t20220527_4148687.shtml |
|
江苏 |
江苏省药品监督管理局同一集团已取得第二类医疗器械注册证产品来苏申报注册工作指南(试行) |
2022-06-30 |
江苏省药品监督管理局 http://da.jiangsu.gov.cn/art/2022/6/30/art_65298_10525240.html |
|
贵州 |
省药品监管局关于印发《关于优化贵州省第二类医疗器械审评审批的若干措施》的通知 |
2022-07-01 |
贵州省药品监督管理局 http://yjj.guizhou.gov.cn/zwgk/gzhgfxwjsjk/gfxwjsjk/202207/t20220701_75363680.html |
|
《关于优化贵州省第二类医疗器械审评审批的若干措施》政策解读 |
2022-07-04 |
贵州省药品监督管理局 http://yjj.guizhou.gov.cn/jdhy/zcjd/wzjd/202207/t20220704_75381940.html |
|
|
辽宁 |
辽宁省药品监督管理局境内第二类医疗器械优先注册程序 |
2022-07-05 |
辽宁省药品监督管理局 -意见征集 http://ypjg.ln.gov.cn/hdjl_133062/zqyj/202207/t20220705_4608368.html |
|
云南 |
省药监局出台 20 条措施促进医疗器械产业高质量发展 |
2022-07-22 |
云南省药品监督管理局 http://mpa.yn.gov.cn/newsite/NewsView.aspx?ID=a358264a-f2ea-4003-a89f-20c4e6a59882 |
|
江西 |
优化营商环境 促进医疗器械产业高质量发展 “十三条”惠企政策 |
2022-09-13 |
【附件】:同一集团、同一法人已取得第二类医疗器械注册证产品来赣申报注册实施细则 http://mpa.jiangxi.gov.cn/art/2022/9/14/art_35392_4141841.html |