在《台湾医疗器械企业如何申报接触镜护理产品注册(一)》中UC讨论了国家药监局( NMPA )对接触镜护理产品的基本法规要求,本文将主要针对有效期研究进行阐述以帮助台湾地区医疗器械企业完成符合国家法规的有效期研究报告。
有效期研究一般可采用加速老化试验方式或是实时老化试验方法。加速老化试验所得的有效期为试验条件下推导得出,一定程度上代表了产品的寿命,但还需进行实时老化加以验证。接触镜护理产品的有效期研究可参考标准YY0719.6 进行。
接触镜护理产品的有效期研究应选取 3 批次样品,若少于 3 批次应说明理由。试验的典型性样品应是最小规格包装的型号,可以覆盖容量大于最小规格 8 倍的样品。
若采用加速老化试验进行研究,则可以选取 25 ± 2 ℃为动力学温度试验均值,老化温度应设置在 45 ℃及以下。加速老化试验推导产品有效期时至少还应提供 3 个月的实时老化试验数据,并且不适用于预期超过 2 年的有效期。有效期的延长应通过实时老化试验数据加以验证。
接触镜护理产品有液态和固态之分,在进行有效期研究时湿度的选择应根据产品剂型有所不同。一般对于固态产品应选择相对湿度较高的条件 ( 如 75% ± 5%) ,而液态产品则更应考虑相对湿度较低的湿度条件(如≤ 40% )。试验条件的选择可参考下图:
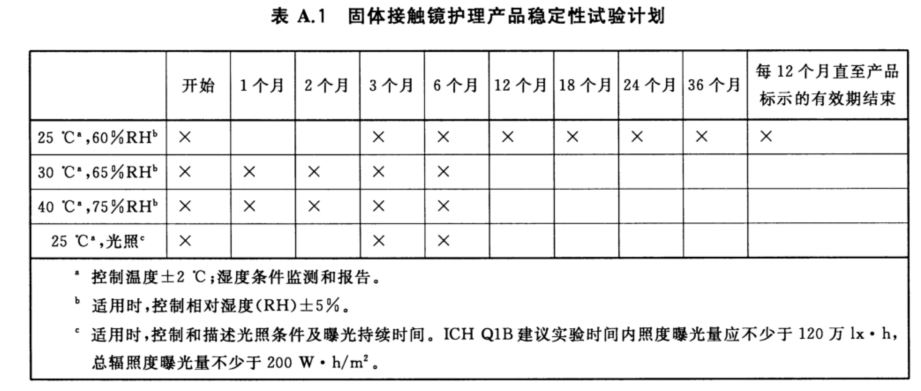
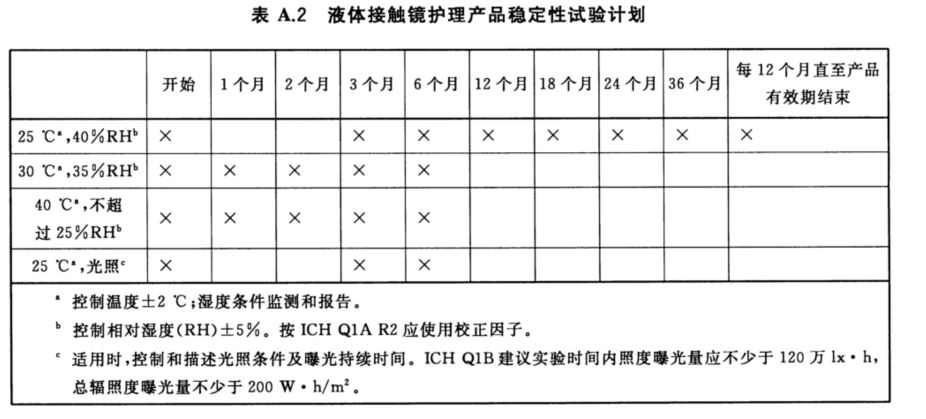
有效期研究时,性能测试的节点也可参考上图选择。测试时应对产品的物理性能(硬度、吸湿性或 PH 、澄清度、颜色等)、化学性能(特别是有效成分含量)、微生物性能(抗微生物活性、防腐有效性、微生物限量)。若无法通过化学方法确定稳定性,也可通过相关性能特性的试验替代,但应说明试验设计理由。
接触镜护理产品根据抗微生物活性的能力被区分为接触镜消毒护理产品和接触镜系统消毒护理产品。前者应当满足直接杀菌试验一类规范,后者应满足直接杀菌试验二类规范及模拟杀菌试验要求。在进行抗微生物活性研究时应至少选取三批次样品,如需进行模拟杀菌试验还应考虑适用的镜片种类,并根据YY 0719.3 分配镜片数量。
接触镜护理产品应验证其在有效期内的防腐有效性和开瓶抛弃周期,应参考 YY0719.4 进行研究。接触镜护理产品的开瓶抛弃周期一般为 28d ,超过 28d 的可按照标准附录的方法进行验证。
接触镜护理产品的有效期研究耗时较长且在产品检测时需要提交有效期研究报告,检测机构需要对企业提供的有效期研究报告进行认可才能完成产品检测,故而接触镜的有效期研究应及早安排。
