新型冠状病毒感染来势汹汹,疫情期间国家药监局和多个省级药品监管部门迅速启动医疗器械应急审批程序,全力保障疫情所需医疗器械产品。
根据2009年国家药监局发布的<<关于印发医疗器械应急审批程序的通知>>,UC可以知道应急审批是为了有效预防、及时控制和消除突发公共卫生事件的危害,确保突发公共卫生事件应急所需医疗器械尽快完成审批的程序。应急审批和UC往常注册的程序相比,其特点是是更快,可以容缺受理,但是有效期较短,一般不超过一年。
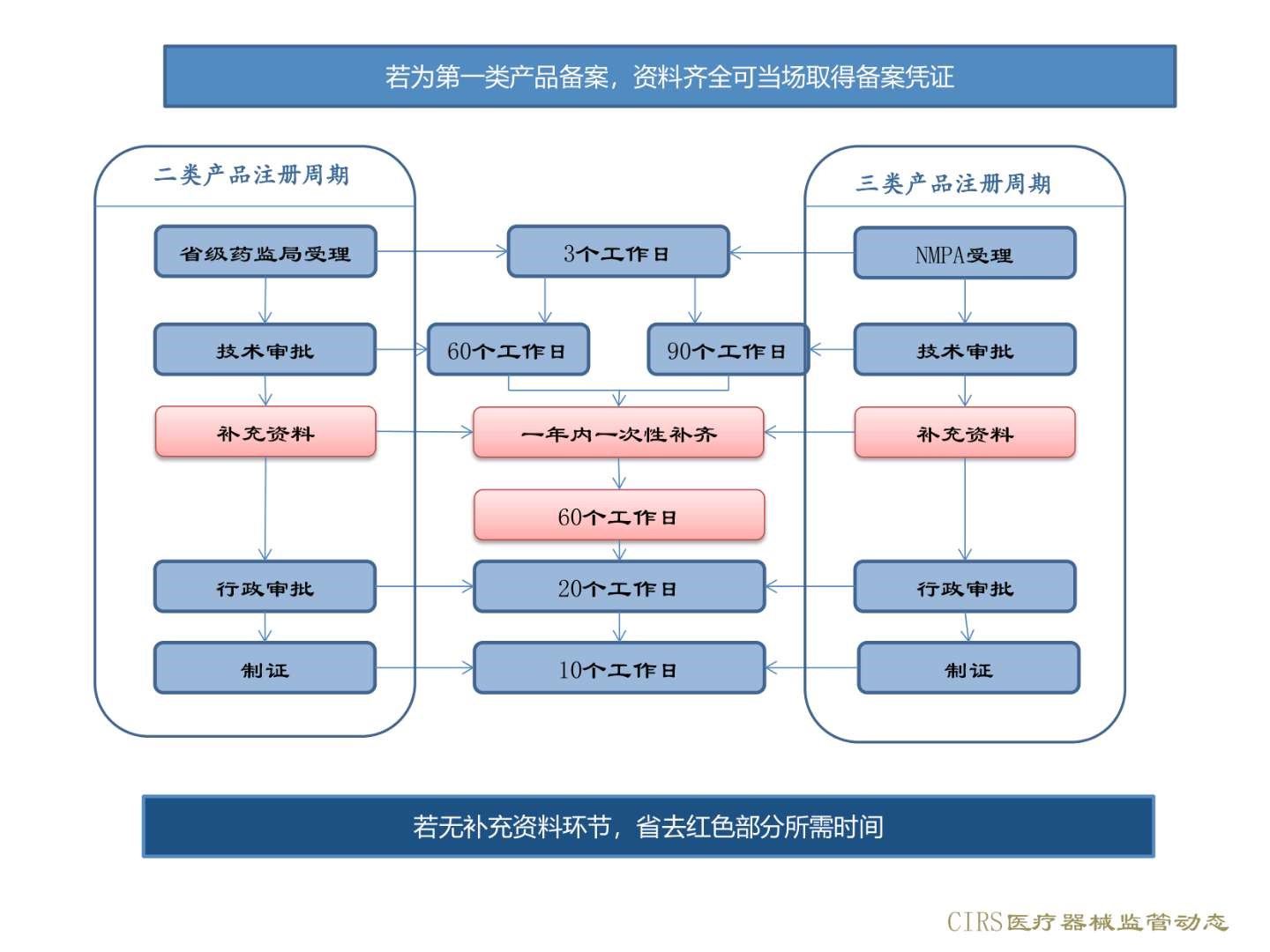
根据国家的文件,UC整理了应急审批流程图,如下:
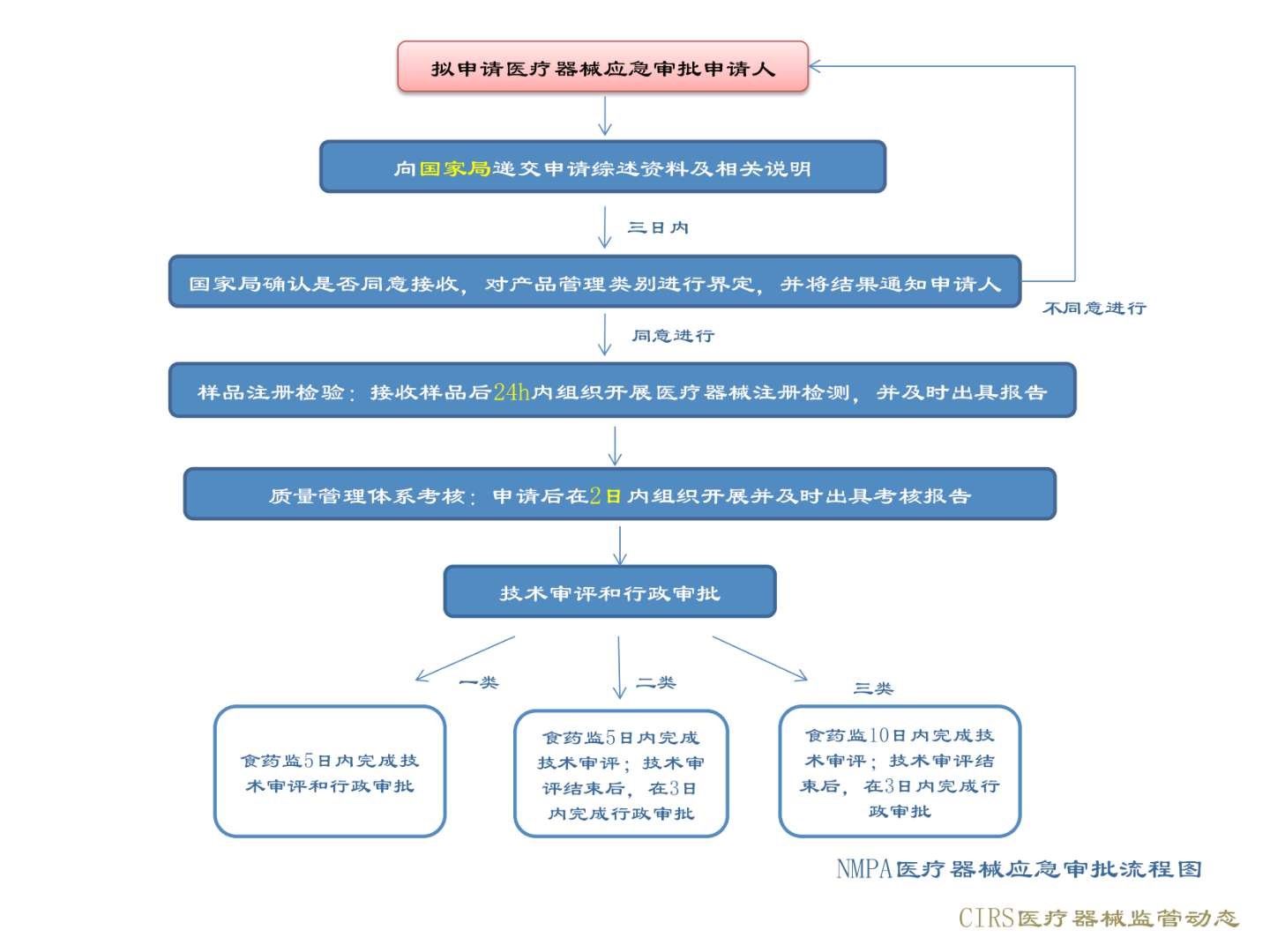
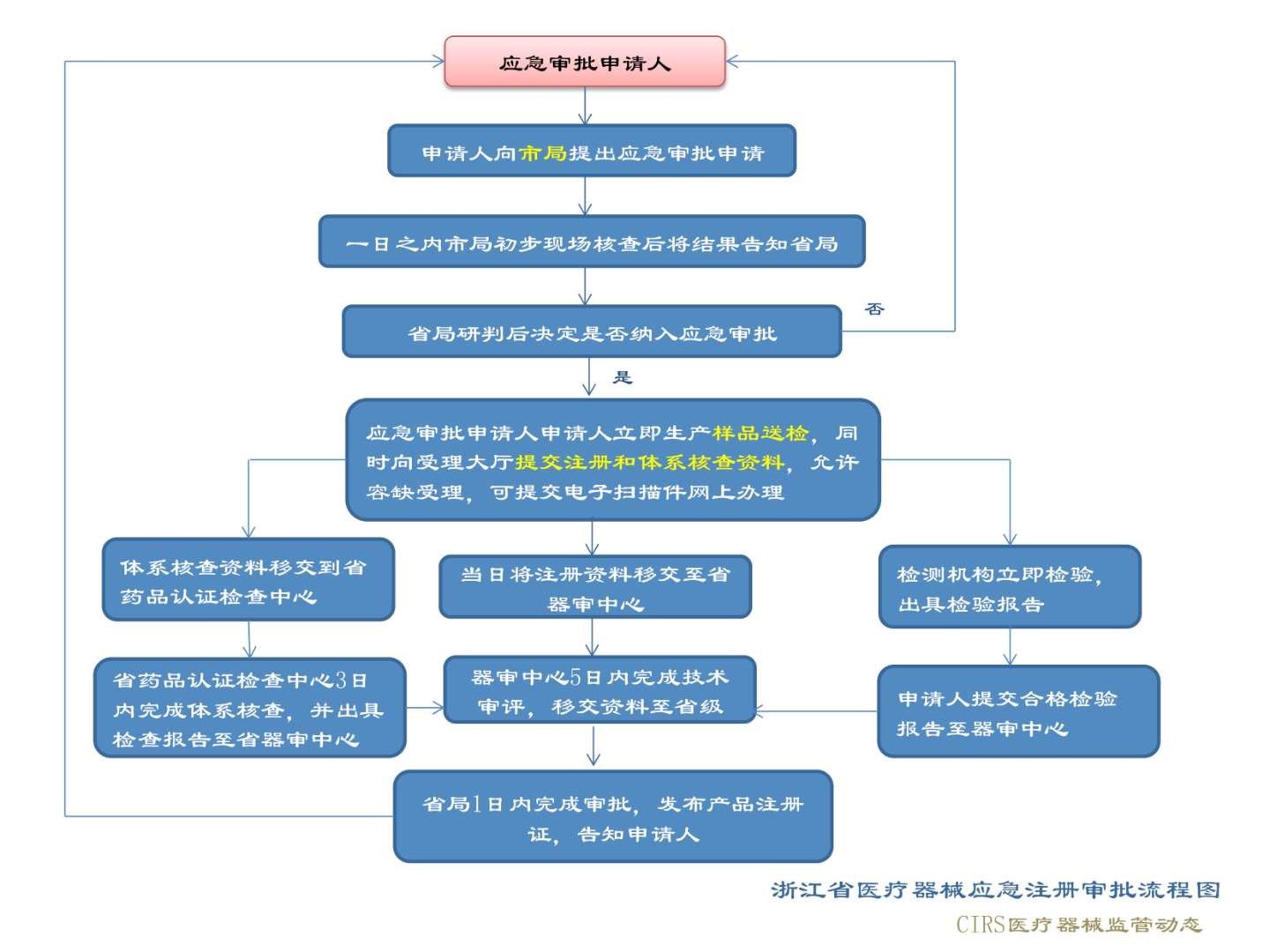
第III类医疗器械向国家药品监督管理局申报,第I类和第II类医疗器械向医疗器械生产企业所在地省、自治区、直辖市药品监督管理局申报。各省的应急审批流程以省市实际发布的医疗器械应急审批程序相关文件为准,比如浙江省药监局发布的流程图:
应急审批已经进入尾声,各省审批通道即将关闭,那么企业如果有产品还想要注册上市,就要按照《医疗器械注册管理办法》进行申报。