自2015年4月1日起,新《医疗器械监督管理条例》(650号令)下医疗器械注册证到期延续注册过渡期结束,所有医疗器械注册证书应在有效期届满6个月前向食品药品监督管理部门提出延续注册申请,而原《条例》规定的重新注册不再适用。
依据新的医疗器械监督管理条例规定,医疗器械注册证书到期前可申请延续注册,取代了原《条例》规定的重新注册申请,新的《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》自2014年10月1日起生效,延续注册也随之正式实施,UC可以从下图了解新《条例》医疗器械延续申请是如何实施。
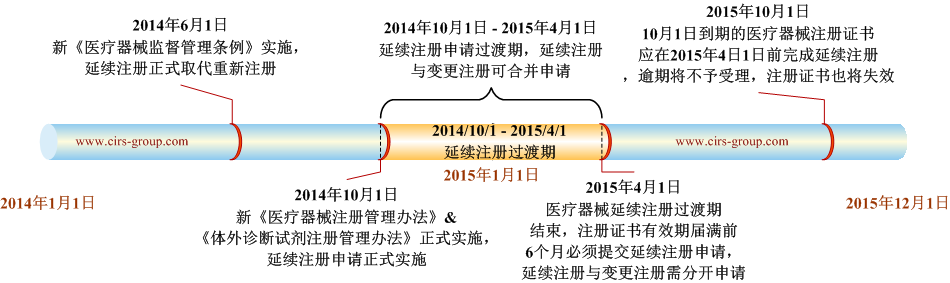
医疗器械企业应关注其中的几个关键时间点:
- 2014年6月1日: 新《医疗器械监督管理条例》正式生效,延续注册取代重新注册;
- 2014年10月1日: 新《医疗器械注册管理办法》和《体外诊断试剂注册管理办法》正式生效,延续注册正式开始实施;
- 2015年4月1日:医疗器械延续注册6个月的过渡期结束,延续注册与变更注册需分开申请;
哪些情况下延续注册申请不被受理:
- 注册人未在规定期限内提出延续注册申请的;
- 医疗器械强制性标准已经修订,该医疗器械不能达到新要求的;
- 对用于治疗罕见疾病以及应对突发公共卫生事件急需的医疗器械,批准注册部门在批准上市时提出要求,注册人未在规定期限内完成医疗器械注册证载明事项的。
注:企业应及时关注医疗器械相关国家标准及行业标准的修订情况,一旦强制性标准修订,企业应及时调整产品技术要求,直到达到新的标准要求。
医疗器械延续注册申报资料要求:
- 申请表 (采用新的申报软件编写)
- 证明性文件,主要包括企业营业执照、组织机构代码证、代理人委托书、代理人承诺书等。
- 关于产品没有变化的声明
- 原医疗器械注册证及其附件的复印件、历次医疗器械注册变更文件复印件
- 注册证有效期内产品分析报告
- 产品临床应用情况,用户投诉情况及采取的措施。
- 医疗器械不良事件汇总分析评价报告,报告应对本产品上市后发生的可疑不良事件列表、说明在每一种情况下生产企业采取的处理和UC。对上述不良事件进行分析评价,阐明不良事件发生的原因并对其安全性、有效性的影响予以说明。
- 在所有国家和地区的产品市场情况说明。
- 产品监督抽验情况(如有)。
- 如上市后发生了召回,应当说明召回原因、过程和处理结果。
- 原医疗器械注册证中载明要求继续完成工作的,应当提供相关总结报告,并附相应资料。
如医疗器械强制性标准已经修订,应提供产品能够达到新要求的产品检验报告。产品检验报告可以是自检报告、委托检验报告或符合强制性标准实施通知规定的检验报告。其中,委托检验报告应由具有医疗器械检验资质的医疗器械检验机构出具。
7. 符合性声明及其它文件1)注册人声明本产品符合《医疗器械注册管理办法》和相关法规的要求;声明本产品符合现行国家标准、行业标准,并提供符合标准的清单。
2)所提交资料真实性的自我保证声明(境内产品由注册人出具,进口产品由注册人和代理人分别出具)。
3)如在原医疗器械注册证有效期内发生了涉及产品技术要求变更的,应当提交依据注册变更文件修改的产品技术要求一式两份。
相关链接:
- 关于医疗器械(含体外诊断试剂)注册申报有关问题的公告(第129号)
- 关于医疗器械延续注册申请过渡期相关问题的公告(第143号)
- 关于医疗器械(含体外诊断试剂)延续注册申报资料有关问题的公告(第144号)
