医用隔离衣作为医用防护类医疗器械,在此次疫情防控过程中发挥了重大的作用,同时也是作为疫情应急物质,瑞旭集团医疗器械服务团队结合国家疫情防控要求及企业需求,紧急协助一批企业完成了医用隔离衣的备案审批 ,结合疫情防控期间应急审批政策,现将医用隔离衣产品的备案要求及流程分享如下:
1 . 医用隔离衣产品概述
- 产品名称: 隔离衣
- 结构组成: 通常采用非织造布为主要原料,经裁剪、缝纫制成。非无菌提供,一次性使用。
- 工作原理 :利用衣物的阻隔作用,保护医务人员避免受到血液、体液和其他感染性物质污染,或用于保护患者避免感染。
- 预期用途: 用于医疗机构门诊、病房、检验室等作普通隔离。
- 适用人群: 适用于各种环境下需要进行防护的人群。
- 预期使用环境: 医疗机构门诊、病房、检验室等。
2. 医用隔离衣主要产商信息
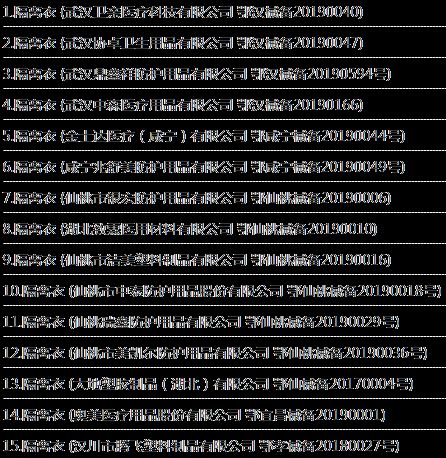
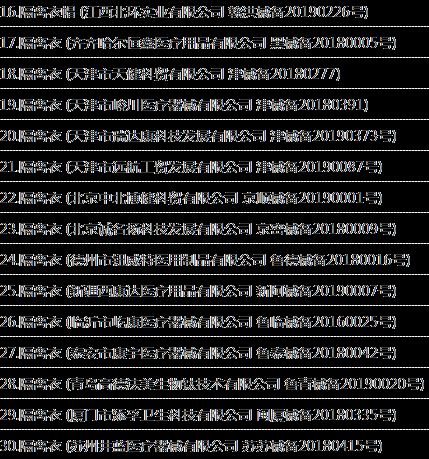
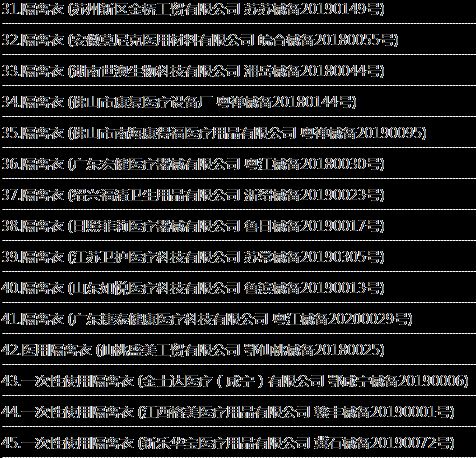

3. 医用隔离衣分类信息
|
子目录 |
一级 |
二级 |
产品描述 |
预期用途 |
品名举例 |
类别 |
|
14 注输、护理和防护器械
|
14 医护人员防护用品 |
03 隔离衣帽 |
通常采用非织造布为主要原料,经裁剪、缝纫制成。非无菌提供,一次性使用。 |
用于医疗机构门诊、病房、检验室等作普通隔离。 |
隔离衣、医用帽 |
Ⅰ |
医用隔离衣按照第一类医疗器械管理,需要根据要求完成医疗器械备案。
4. 医用隔离衣临床试验要求
免临床:一类医疗器械,不需要做临床试验
5. 医用隔离衣技术要求
5.1 外观
1) 隔离衣应干燥、清洁、无霉斑,表面不允许有黏连、裂缝、孔洞等缺陷。
2) 隔离衣连接部位可采用针缝、粘合或热合等加工方式。针缝的针眼应密封处理,针距每 3cm应为8~14针,线迹应均匀、平直,不得有跳针。粘合或热合等加工处理后的部位,应平整、密封,无气泡。
3) 装有拉链的防护服拉链不能外漏,拉头应能自锁。
5.2结构
1) 隔离衣的结构应合理,穿脱方便,结合部位严密。
2) 袖口、脚踝口采用弹性收口,帽子面部收口及腰部采用弹性收口、拉绳收口或搭扣。
5.3号型规格
医用隔离衣型号通常分为 160、165、170、175、180、185,号型规格见表1和表2。(参考GB 19082-2009医用一次性防护服技术要求)
表 1 连身式号型规格
单位为厘米
|
号型 |
身长 |
胸围 |
袖长 |
袖口 |
脚口 |
|
160 |
165 |
120 |
84 |
18 |
24 |
|
165 |
169 |
125 |
86 |
18 |
24 |
|
170 |
173 |
130 |
90 |
18 |
24 |
|
175 |
178 |
135 |
93 |
18 |
24 |
|
180 |
181 |
140 |
96 |
18 |
24 |
|
185 |
188 |
145 |
99 |
18 |
24 |
|
偏差 |
±2 |
±2 |
±2 |
±2 |
±2 |
表 2 分身式号型规格
单位为厘米
|
号型 |
上衣长 |
胸围 |
裤长 |
腰围 |
|
160 |
76 |
120 |
105 |
100~105 |
|
165 |
78 |
125 |
108 |
105~110 |
|
170 |
80 |
130 |
111 |
110~115 |
|
175 |
82 |
135 |
114 |
115~120 |
|
180 |
84 |
140 |
117 |
120~125 |
|
185 |
86 |
145 |
120 |
125~130 |
|
偏差 |
±2 |
±2 |
±2 |
±2 |
5.4抗湿性
外侧面沾水等级不低于 3级要求。
5.5断裂强力
隔离衣关键部位材料的断裂强力应不小于 45N。
5.6断裂伸长率
隔离衣关键部位材料的断裂伸长率应不小于 15%。
5.7微生物
符合 GB 15979-2002中微生物指标的要求,见表3。
表 3 微生物指标
|
细菌菌落总数CFU/g |
大肠菌群 |
绿脓杆菌 |
金黄色葡萄球菌 |
溶血性链球菌 |
真菌菌落总数CFU/g |
|
≤200 |
不得检出 |
不得检出 |
不得检出 |
不得检出 |
≤100 |
6. 医用隔离衣适用的技术标准
|
GB/T 191-2008 |
包装储运图示标志 |
|
GB 19082-2009 |
医用一次性防护服技术要求 |
|
GB/T 3923.1-2013 |
纺织品 织物拉伸性能 第1部分 断裂强力和断裂伸长率的测定(条样法) |
|
GB/T 3923.2-2013 |
纺织品 织物拉伸性能 第2部分 断裂强力的测定(抓样法) |
|
GB/T 4745-2012 |
纺织品 防水性能的检测和评价 沾水法 |
|
GB 15979-2002 |
一次性使用卫生用品卫生标准 |
7.医用隔离衣备案时限
医用隔离衣作为 I类医疗器械,备案制,现场提交备案资料,现场审核通过后,当场发放医用隔离衣备案凭证。
其中医用隔离衣备案凭证含两部分内容:第一类医疗器械备案凭证和第一类医疗器械备案信息表。
