根据我国法规要求,注册类保健食品所声称的保健功能应当已经列入保健食品功能目录。目前,我国拟定的保健食品功能共有24个,企业需从允许声称的保健食品功能目录中选择与产品相匹配的功能。
为了进一步规范允许保健食品声称的保健功能目录的管理工作,国家市场监督管理总局发布并实施了《保健食品原料目录与保健功能目录管理办法》和《保健食品新功能及产品技术评价实施细则(试行)》,正式开放保健食品新功能的申报,推动保健食品新功能创新。
保健食品新功能的法规现状
|
法规文件 |
实施日期 |
|
《保健食品原料目录与保健功能目录管理办法》 |
2019年10月1日 |
|
《保健食品新功能及产品技术评价实施细则(试行)》 |
2023年8月28日 |
保健食品新功能建议人的资质要求
- 保健食品新功能建议人可为任何单位或者个人。
- 任何单位或者个人在开展相关研究的基础上,可以单独或联合向国家市场监督管理总局食品审评中心提出新功能建议。
保健食品新功能的定位
保健食品新功能定位应当明确,分为以下三类:
1. 补充膳食营养物质
2. 维持或改善机体健康状况
3. 降低疾病发生风险因素
保健食品新功能的申报流程
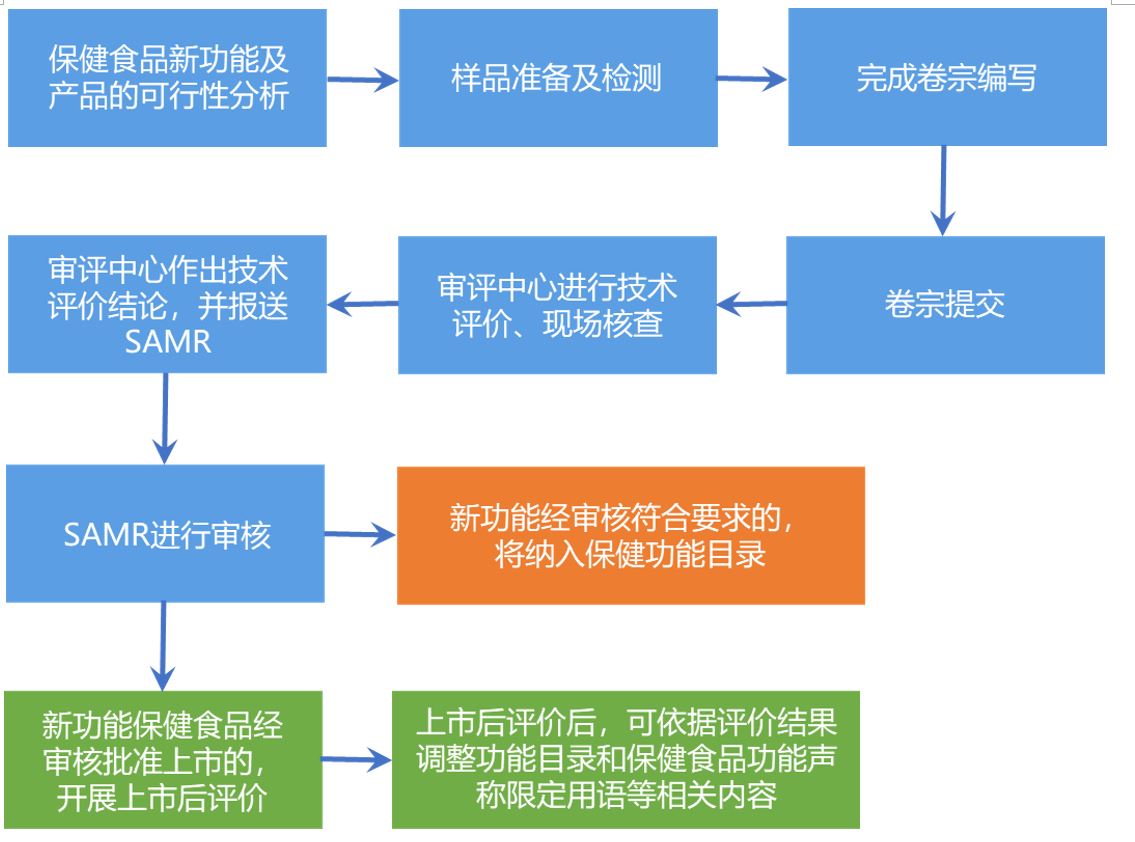
注:建议人同步提出新功能建议和对应的新功能保健食品注册申请的,食品审评中心应当同步接收,开展关联审评。
申报资料的要求
保健食品新功能的申报材料要求
建议人提交新功能建议时,应当按照《实施细则》附表“保健食品新功能建议材料项目要求和技术评价要点”提供技术评价材料,具体材料项目为:
1. 新功能建议材料目录
2. 建议人对提交材料真实性负责的承诺书
3. 建议人身份证明或主体登记证明文件复印件
4. 保健功能名称、解释、机理及其依据
5. 保健功能研究报告
6. 保健功能评价方法及验证评价资料
7. 相同或者类似保健功能在国内外的应用情况
8. 有助于技术评价的科学文献依据及其他相关材料
9. 保健功能伦理学相关材料
10. 新功能研究样品技术评价相关材料
11. 其他与功能建议和评价相关的材料
12. 其他人群试食试验评价相关资料
13. 其他需要说明的问题
新功能保健食品的注册申请材料要求
申请人提交新功能保健食品注册申请时,应当按照 保健食品注册管理相关规定 提交申请材料,申请人资质应当符合要求。
UC的服务
瑞旭其他热门服务:
更多法规报告免费获取:
- 免费获取!2022年食品法规及行业热点年度盘点报告 (点击查看)
详细版的《2022年食品法规及行业热点年度盘点报告》将分为六大板块:
1. 食品安全国家标准的制修订动态;
2. 特殊食品法规汇总报告(批准动态+法规动态);
3. 三新食品:重点原料合规进展(母乳低聚糖HMOs等)
4. 食品安全抽检情况
5. 行业关注热点(NMN,功能性食品及其原料,后生元等)
6. 食品安全违法案例
相关阅读:

