UC 第I类医疗器械备案
依据《医疗器械监督管理条例》规定,第I类医疗器械施行备案管理,进口UC 第I类医疗器械备案人向国家药品监督管理部门提交备案资料,国产UC 第I类医疗器械备案人向所在地设区的市级药品监督管理部门提交备案资料。
UC 第I类医疗器械备案流程
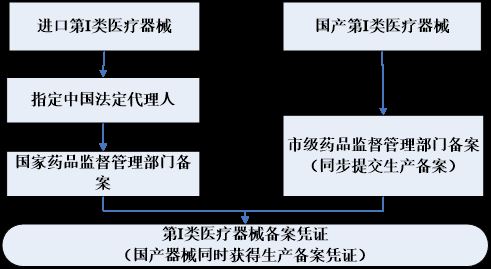
UC的服务
-
产品技术要求及说明书编制审核
-
产品全性能检测服务
-
生产质量管理体系辅导
-
医疗器械产品备案
-
医疗器械生产备案
扫描下方的二维码订阅“
CIRS医械合规动态
”!实时传递最新医疗器械监管法规动态,分享医疗器械注册成功经验及经典案例跟踪医疗器械最新产品安全与法规监管动态,获得最新一手资讯。

① 凡本网注明"稿件来源:“杭州瑞旭科技集团有限公司"的所有文字、图片和音视频稿件,版权均属杭州瑞旭科技集团有限公司所有,任何媒体、网站或个人未经本网协议授权不得转载、链接、转贴或以其他方式复制发表。已经本网协议授权的媒体、网站,在下载使用时必须注明"稿件来源:杭州瑞旭科技集团有限公司",违者本网将依法追究责任。
② 本网未注明"稿件来源:杭州瑞旭科技集团有限公司 "的文/图等稿件均为转载稿,本网转载出于传递更多信息之目的,并不意味着赞同其观点或证实其内容的真实性。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。如擅自篡改为"稿件来源:杭州瑞旭科技集团有限公司",本网将依法追究责任。如对稿件内容有疑议,请及时与UC联系。
③ 如本网转载稿涉及版权等问题,请作者在两周内速来电或来函与杭州瑞旭科技集团有限公司联系。

