CDMO服务介绍
医疗器械注册人制度(MAH)全面实施,即允许医疗器械注册人(注册证持有人)通过委托合规的生产平台的方式获得产品注册审批上市,从而优化了资源配置,加快创新医疗器械产品上市进程。
瑞旭集团基于医疗器械注册人制度打造了合规的专业研发生产服务平台-瑞旭医疗器械产业转化CDMO平台,致力于为进口医疗器械国产化、科研成果产业转化、政府引导项目转化、研发生产资源整合项目及初创期器械项目提供法规咨询、技术转化、样品生产、检测验证、临床评价(试验)、质量体系及注册申报(认证)等全产业链技术服务。帮助创新医疗器械企业减少研发生产运营成本、缩短产品上市周期、提升项目转化成功率、提高产品注册通过率,高效推进医疗器械的产业化。
医疗器械产业化全流程技术服务
瑞旭集团通过整合原有医疗器械检验检测、质量体系、临床前动物实验、临床试验、注册申报等业务,将服务链向上游延伸,将医疗器械研发和生产外包服务纳入到瑞旭集团医疗器械技术服务体系,致力于为国内外医疗器械企业提供从研发生产到临床注册全产业技术服务。
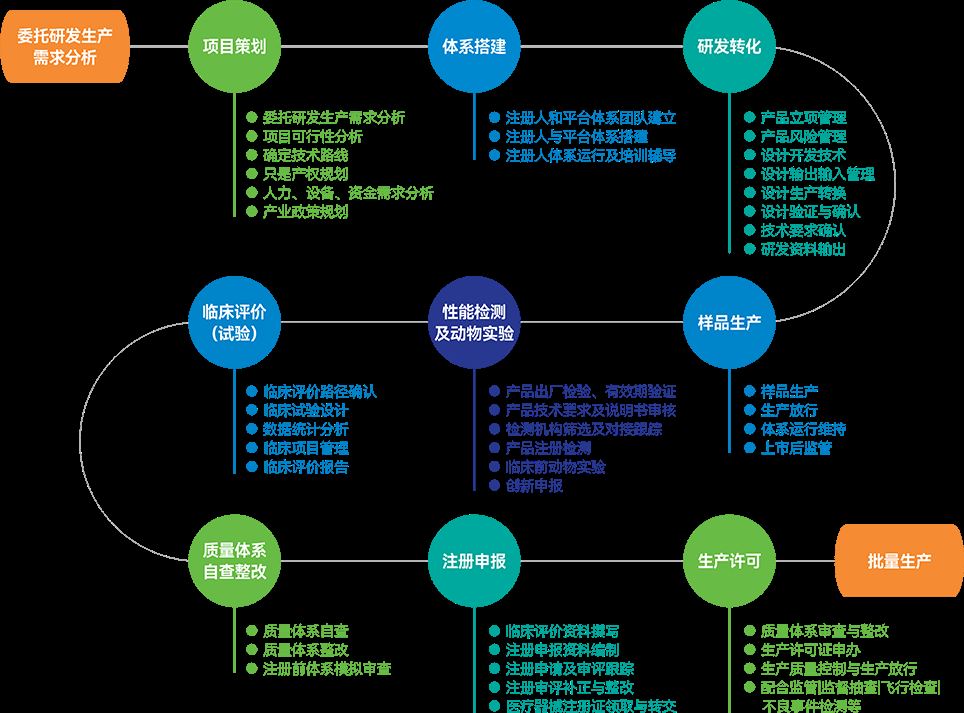
CDMO服务模式
从概念到产品产业化合规上市

CDMO服务领域
-
进口医疗器械本地化生产
-
进口医疗器械国产化替代
-
高校及科研院所的医疗器械技术成果产业化转化
-
政府引导的创新医疗器械项目产业化
-
注册人制度下研发生产资源重新整合的项目
-
其它有需求的创新医疗器械产业化及市场准入
CDMO服务内容

CDMO服务优势
-
专业的研发生产平台
瑞旭CDMO平台配置有专业研发生产平台,其中9个无菌生产车间共计4600㎡, 非无菌生产车间3个,配置结构设计实验室、有源器械研发实验室、医用耗材研发实验室、理化实验室、微生物及无菌实验室。可满足各类医疗器械的研发和生产 。

-
成熟的技术及运营管理团队
瑞旭CDMO平台配备医疗器械产业化项目管理、研发、生产、检验、质量体系、临床、注册等专业技术团队,其中核心团队90%在医疗器械行业具有10年以上从业经验,涉及消化、泌尿、妇科、骨科、肝胆外科、整形外科、神经外科、呼吸科等领域器械产品的研发、生产、体系、临床和注册成功经验。

-
丰富医疗器械研发生产经验
平台拥有自主研发和生产的多项创新医疗器械产品,已经成功通过审查并获得医疗器械注册证和生产许可证。

-
完善的产业政策和渠道资源
平台与科技政策咨询平台、创新医疗器械孵化器、产业基金、科研机构等多渠道建立合作,为医疗器械注册人提供公司注册、技术转化、专利申报、项目申报、投融资咨询、专业辅导、人才培养、项目孵化等配套服务。
联系UC
杭州瑞旭科技集团有限公司
北 京:010-6398 4062 15010201703
杭 州:0571-8720 6527 13588404338
邮 箱:md@hfoushi.com
网 址: www.hfoushi.com
总部地址:杭州市滨江区秋溢路288号东冠高新科技园1号楼11层
CDMO地址:杭州市余杭区瓶窑镇岭上路2号(莱恩瑟特医疗园区内)
